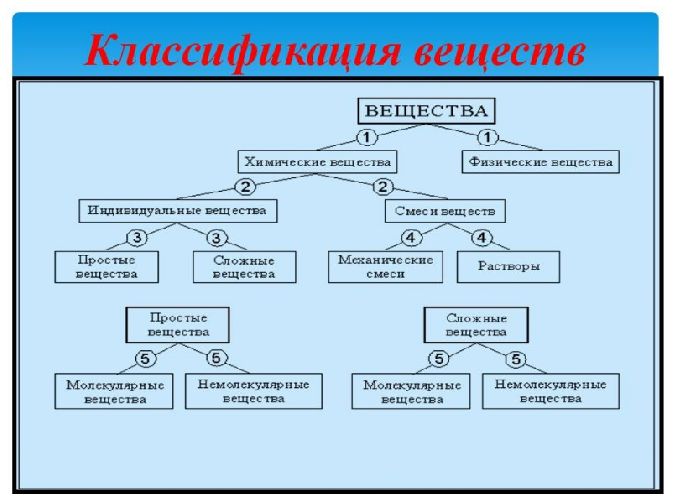
Урок №51. Генетическая связь между основными классами неорганических соединений
Генетические связи — это связи между разными классами, основанные на их взаимопревращениях.
Зная классы неорганических веществ, можно составить генетические ряды металлов и неметаллов. В основу этих рядов положен один и тот же элемент.
Среди металлов можно выделить две разновидности рядов:
1 . Генетический ряд, в котором в качестве основания выступает щёлочь. Этот ряд можно представить с помощью следующих превращений:
металл→основный оксид→щёлочь→соль
Например, K→K 2 O→KOH→KCl
2 . Генетический ряд, где в качестве основания выступает нерастворимое основание, тогда ряд можно представить цепочкой превращений:
металл→основный оксид→соль→нерастворимое основание→основный оксид→металл
Например, Cu→CuO→CuCl 2 →Cu(OH) 2 →CuO→Cu
Среди неметаллов также можно выделить две разновидности рядов:
1 . Генетический ряд неметаллов, где в качестве звена ряда выступает растворимая кислота. Цепочку превращений можно представить в следующем виде:
неметалл→кислотный оксид→растворимая кислота→соль
Например, P→P 2 O 5 →H 3 PO 4 →Na 3 PO 4
2 . Генетический ряд неметаллов, где в качестве звена ряда выступает нерастворимая кислота:
неметалл→кислотный оксид→соль→кислота→кислотный оксид→неметалл
Например, Si→SiO 2 →Na 2 SiO 3 →H 2 SiO 3 →SiO 2 →Si
Генетическая связь.
Все типичные классы соединений находятся в генетической связи друг с другом.
Рассмотрим схему генетических связей:
В верхней части схемы генетических связей расположены 2 группы простых веществ – металлы и неметаллы, а также водород, строение атома которого отличается от строения других атомов элементов. На валентной оболочке атома водорода находится 1 электрон, как у элементов 1й группы (щелочных металлов), но в то же время ему не хватает 1го электрона для завершения внешнего уровня, как у галогенов.
Волнистая черта разделяет сложные вещества от простых. Любая реакция, в которой участвуют вещества, находящиеся по разную сторону от этой черты, будут носить окислительно-восстановительный характер.
В левой части под металлами расположены их типичные соединения – оксиды и основания, в правой части находятся соединения, типичные для неметаллов – кислотные оксиды и кислоты. Водород, находящийся посредине, дает очень специфический амфотерный оксид – воду Н2О, которая в сочетании с основным оксидом дает основание, а с кислотным – кислоту.
В основном, в химические реакции вступают соединения, принадлежащие к разным частям схемы генетической связи.
Химия
План урока:
Почему связь между классами веществ считается генетической
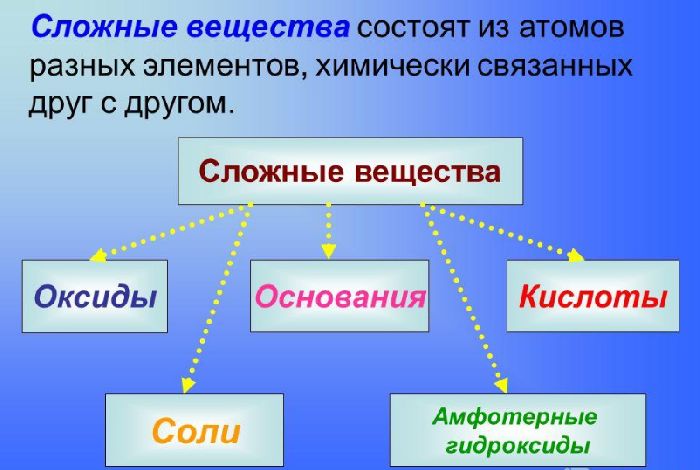
Чтобы разобраться в этом вопросе. Вспомним состав классов веществ, с которыми Вы познакомились на предыдущих занятиях.
Обратите внимание, что соли содержат в себе частицы как оснований (атомы металла), так и кислот (кислотных остатков). Если соль рассматривать как «венец» превращений, то давайте, попытаемся прийти к истокам. Всё начинается с простого, точнее металла и неметалла, как простых веществ.
Попробуем построить генетический ряд металлов, переходя от одного класса к другому.
Возьмём, к примеру, металлы кальций и медь, подставив их в цепочку уравнений.
Обратите внимание, что данные металлы отличаются своей реакционной способностью.
Получается, эта генетическая связь соединений присуща только для активных металлов, оксиды которых, реагируя с водой, дают продукт в виде щёлочи.
Для металлов, которые отличаются малой активностью, переход от вещества, находящегося в простом состоянии, к соли, происходит путём превращений.
Поскольку основные оксиды реагируют с металлами (более активными, чем металлы, которые входят в состав оксида), то эту схему можно сократить.
Аналогичным способом можно составить генетический ряд неметаллов, начиная от неметалла заканчивая солью или неметаллом.
Подставим в цепочку уравнений фосфор и кремний.
А возможны иные пути решения данных цепочек уравнений. Способы получения кислотных оксидов реализуются путём взаимодействия простых веществ с кислородом. А вот не с каждого оксида можно получить ему соответствующую кислоту, путём прибавления воды. Поскольку кремниевая кислота нерастворима в воде, то необходимо получить сначала соль, а потом уже и кислоту.
В данном решении предлагается добыть соль Na3PO4, взаимодействием основания и кислоты. Однако можно использовать и другие варианты, которые также будут верны.
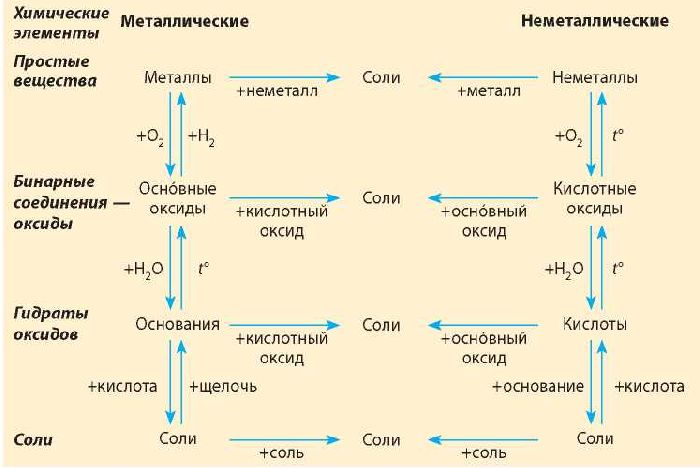
Если объединить генетические ряды металлов и неметаллов, получим дружную семью неорганических соединений, где каждое вещество связано неразрывной нитью с другими классами. Таблица 1.
Данная таблица отображает, как реагируют между собой вещества и какие продукты возможны, вследствие реакции.
Промоделируем на примере: В вашем распоряжении имеются следующие вещества: оксид серы (VI), гидроксид бария, соляная кислота, карбонат кальция и железо. Ваша задача спрогнозировать, между какими соединениями возможна реакция и, записать, соответствующие уравнения реакций.
Подтвердив свои прогнозы молекулярно-ионными уравнениями в сокращённом и полном виде.
Родственные связи между металлами и неметаллами
Кислород является типичным представителем неметаллов. Он является достаточно сильным окислителем, перед которым может устоять только фтор. Получение основных оксидов происходит путём взаимодействия кислорода и металлов. Однако не все металлы охотно с ним реагируют. Щелочные реагируют бурно, именно поэтому их хранение осуществляется под слоем керосина. Необходимо заметить, что щелочные металлы не образуют оксиды во время взаимодействия с О2. Их чрезвычайная активность позволяет получать только для их характерные продукты, это будут пероксиды и надпероксиды (за исключением лития, продукт Li2O).
А вот, чтобы менее активные металлы – железо или медь прореагировали, необходимо нагревание.
Получение кислотных оксидов происходит аналогично взаимодействием неметаллов с О2.
Металлы и неметаллы в химии рассматриваются как противоположности, которые, как заряды (положительные и отрицательные) имеют свойства притягиваться. Рассмотрим на примере металла кальций и неметалла углерод.
Соль СаСО3 имеет истоки от простых веществ Са и С, промежуточным звеном являются оксиды этих веществ, для которых свойственно реагировать между собой.
Вспомним с Вами один с основных постулатов химии, а именно, закон постоянства состава вещества.
Представим, что мы с Вами химики-первооткрыватели и нам предстоит сложная задача получить азотную кислоту, которая имеет важную роль в химической промышленности. Получение кислот возможно несколькими способами. Обращаясь к таблице 1, делаем вывод, что нам доступно несколько способов, а именно.
Взаимодействие кислот с солями приведёт нас к желаемому результату, однако не забывайте, что в продукте должны увидеть газ, осадок либо окрашивание.
Способы получения средних солей доказательно показывают связь между веществами. Снова выручалочкой нам послужит таблица 1. Наша задача получить вещество, без которого, полагаем, Вы не представляете своё существование, это соль NaCl. Используя данные, видим, что доступно для её получения 4 способа (Вы ищете, где продуктом является соль и применяете данные на свой пример).
Рассмотрим подробно каждый с них.
Способы получения солей отличаются, причиной этому является то, какую именно соль мы хотим получить, кислородсодержащей,сильной или слабой кислоты. К примеру, получение Na2SO4 будет отличаться от предыдущего примера с NaCl. Количество способов будет больше, так как это соль кислородсодержащей кислоты.
Здесь следуют отметить особенность щелочных, а также щелочно-земельных металлов, для которых свойственно взаимодействие с водой. По сути, идёт два параллельных процесса.
Полученная щёлочь реагирует с кислотой.
Способы получения солей аммония несколько отличаются, от солей металлов, тем, что аммиак непосредственно реагирует с кислотами (смотри урок химическая связь) с образованием донорно-акцепторных связей.
Гидроксид аммония имеет способность взаимодействовать с кислотами, с образованием необходимого продукта, не иначе как солей аммония.
Наверняка некоторые из Вас пугал вид заданий, который был цепочек уравнений. Обобщая всё выше сказанное, рассмотрим несколько примеров.
Чтобы справится с данной задачей, проанализируем условие. Первое, что необходимо выделить – это количество уравнений (смотрим по стрелочкам, их 5). Второе определим исходное вещество – цинк, металл средней силы. Чтобы получить с него соль (не забываем о таблице 1), можно использовать 3 способа:
Выбор за Вами, одного из трёх уравнений. Переходим к следующей части цепочки ZnCl2 → Zn(OH)2. Здесь решением будет один вариант, это прибавление щёлочи.
Zn(OH)2 относится к нерастворимым основанием, поэтому при нагревании распадаются.
И наконец, итоговый продукт, металл. Его необходимо выделить из соли. Для этого необходимо взять металл, сила которого будет больше. Если эту информацию забыли, то освежить эти данные сможете с помощью урока Соли и их свойства.
Решение цепочек химических уравнений на первый взгляд кажется не посильной задачей, но если внимательно изучить свойства веществ, то они кажутся не такими уж и сложными.
Взаимопревращение между классами веществ
Обобщая сведения о свойствах неорганических соединений, составим схему 1. Взаимосвязь между классами неорганических веществ.
Эта схема и таблица 1 будут служить Вам волшебной палочкой в изучении неорганической химии.
http://www.calc.ru/Geneticheskaya-Svyaz.html
http://100urokov.ru/predmety/urok-12-prevrashheniya-mezhdu-veshhestvami
Генетический ряд металла состоит из простого вещества, оксида, гидроксида и соли:
металл — основный оксид — основание — соль.
Все металлы можно разделить на две группы: активные и неактивные.
К активным относят металлы, реагирующие с водой при обычных условиях. Это (10) металлов: литий, натрий, калий, рубидий, цезий, франций, кальций, стронций, барий, радий. Их оксиды соединяются с водой с образованием растворимых гидроксидов — щелочей.
Остальные металлы менее активны. Их оксиды не реагируют с водой, а основания в воде не растворяются. Поэтому из оксида получить основание можно только через соль. Для неактивных металлов генетический ряд выглядит так:
металл — основный оксид — соль1 — основание — соль2.
1. Генетические ряды активных металлов:
Ряд лития:
Li→Li2O→LiOH→Li2SO4
.
Ряд кальция:
Ca→CaO→Ca(OH)2→CaCO3
.
Ряд бария:
Ba→BaO→Ba(OH)2→Ba3(PO4)2
.
Составим уравнения для генетического ряда бария:
.
Обрати внимание!
Превращение гидроксида бария в фосфат можно осуществить также с помощью кислотного оксида или растворимой соли:
,
.
2. Генетические ряды неактивных металлов:
Ряд магния:
Mg→MgO→MgCl2→Mg(OH)2→MgSO4
.
Ряд железа:
Fe→FeO→FeSO4→Fe(OH)2→Fe(NO3)2
.
Ряд меди:
Cu→CuO→Cu(NO3)2→Cu(OH)2→CuCl2
.
Составим уравнения реакций для ряда меди:
,
Обрати внимание!
В ряду неактивного металла получить соль из основания можно только с помощью кислоты.
Генетическая связь между классами неорганических веществ

4.7
Средняя оценка: 4.7
Всего получено оценок: 574.
4.7
Средняя оценка: 4.7
Всего получено оценок: 574.
Родство и взаимосвязь химических превращений подтверждается генетической связью между классами неорганических веществ. Одно простое вещество в зависимости от класса и химических свойств образует цепочку превращений сложных веществ – генетический ряд.
Неорганические вещества
Соединения, не имеющие углеродного скелета, характерного для органических веществ, называются неорганическими или минеральными веществами. Все минеральные соединения классифицируются на две обширные группы:
- простые, состоящие из атомов одного элемента;
- сложные, включающие атомы двух и более элементов.
К простым соединениям относятся:
- металлы (K, Mg, Ca);
- неметаллы (O2, S, P);
- инертные газы (Kr, Xe, Rn).
Сложные вещества имеют более разветвлённую классификацию, приведённую в таблице.
|
Класс |
Подкласс |
Примеры |
|
Оксиды |
Основные |
CaO, Na2O |
|
Кислотные |
CO2, SO3 |
|
|
Амфотерные |
ZnO, Al2O3 |
|
|
Гидроксиды |
Нерастворимые основания |
Mg(OH)2, Cu(OH)2 |
|
Щёлочи |
NaOH, Ba(OH)2 |
|
|
Амфотерные |
Zn(OH)2, Fe(OH)3 |
|
|
Кислоты |
Бескислородные |
HCl, H2S, HCN |
|
Кислородсодержащие |
HNO3, H2SO4 |
|
|
Соли |
Основные (комплексные) |
Zn(OH)Cl, Cu2(OH)2CO3 |
|
Кислые |
NaHSO3, CaHPO4 |
|
|
Средние |
Na2SO4, Ca3(PO4)2 |
Амфотерные металлы образуют соответствующие оксиды и гидроксиды. Амфотерные соединения проявляют свойства кислот и оснований.
Генетические ряды
Простые вещества – металлы и неметаллы – образуют цепочки превращений, отражающие генетическую связь неорганических веществ. Посредством химических реакций присоединения, замещения и разложения образуются новые более простые или сложные соединения.
Каждое звено цепочки связано с предыдущим наличием простого вещества. Различие между двумя типами генетических рядов заключается в реакции с водой: металлы образуют растворимые и нерастворимые основания, неметаллы – кислоты.
Основные цепочки превращений описаны в таблице.
|
Вещество |
Генетический ряд |
Примеры |
|
Металл |
Активный металл → основный оксид → щёлочь → соль |
– 2Са + О2 → 2CaO; – CaO + Н2О → Ca(ОН)2; – Ca(ОН)2 + 2HCl → CaCl2 + 2H2O |
|
Малоактивный металл → основный оксид → соль → нерастворимое основание → основный оксид → металл |
– 2Cu + O2 → 2CuO; – CuO + 2HCl → CuCl2 + H2O; – CuCl2 + 2KOH → Cu(OH)2 + 2KCl; – Cu(OH)2 → CuO + H2O; – CuO + H2 → Cu + H2O |
|
|
Неметалл |
→ кислотный оксид → растворимая (сильная) кислота → соль |
– 4P + 5O2 → 2P2O5; – P2O5 + 3H2O → 2H3PO4; – H3PO4 + 3NaOH → Na3PO4 + 3H2O |
|
→ кислотный оксид → соль → нерастворимая (слабая) кислота → кислотный оксид → неметалл |
– Si + O2 → SiO2; – SiO2 + 2NaOH → Na2SiO3 + H2O; – Na2SiO3 + 2HCl → H2SiO3 + 2NaCl; – H2SiO3 → SiO2 + H2O; – SiO2 + 2Zn → 2ZnO + Si |
С помощью цепочки превращения можно получить средние (нормальные) или кислые соли. Комплексные соли могут включать несколько атомов металлов и неметаллов.
Что мы узнали?
Генетическая связь показывает взаимосвязь между классами неорганических веществ. Она характеризуется генетическим рядом – чередой превращений простых веществ. К простым веществам относятся металлы и неметаллы. Металлы образуют растворимые и нерастворимые основания в зависимости от активности. Неметаллы превращаются в сильные или слабые кислоты. Новые сложные вещества ряда образуются реакциями присоединения, замещения и разложения.
Тест по теме
Доска почёта

Чтобы попасть сюда — пройдите тест.
-
Данил Якимов
5/5
-
Сёма Семёнов
5/5
-
Максим Александров
5/5
-
Галина Тимина
4/5
Оценка доклада
4.7
Средняя оценка: 4.7
Всего получено оценок: 574.
А какая ваша оценка?
Генетическая связь между основными классами неорганических соединений
I. Учебный видео-фильм: “Генетическая связь между отдельными классами неорганических соединений”
II. Генетический ряд металлов
Зная классы неорганических веществ, можно составить генетические ряды металлов и неметаллов. В основу этих рядов положен один и тот же элемент.
Генетические связи — это связи между разными классами, основанные на их взаимопревращениях.
Среди металлов можно выделить две разновидности рядов:
1. Генетический ряд, в котором в качестве основания выступает щёлочь. Этот ряд можно представить с помощью следующих превращений:
металл→основный оксид→щёлочь→соль
Например, K→K2O→KOH→KCl
2. Генетический ряд, где в качестве основания выступает нерастворимое основание, тогда ряд можно представить цепочкой превращений:
металл→основный оксид→соль→нерастворимое основание→
→основный оксид→металл
Например, Cu→CuO→CuCl2→Cu(OH)2→CuO→Cu
III. Генетический ряд неметаллов
Среди неметаллов также можно выделить две разновидности рядов:
1. Генетический ряд неметаллов, где в качестве звена ряда выступает растворимая кислота. Цепочку превращений можно представить в следующем виде:
неметалл→кислотный оксид→растворимая кислота→соль
Например, P→P2O5→H3PO4→Na3PO4
2. Генетический ряд неметаллов, где в качестве звена ряда выступает нерастворимая кислота:
неметалл→кислотный оксид→соль→кислота →кислотный оксид→неметалл
Например, Si→SiO2→Na2SiO3→H2SiO3→SiO2→Si
IV. Закрепление
Осуществите превращения по схеме, укажите типы реакций, назовите вещества
1.Al→Al2O3→AlCl3→Al(OH)3→Al2O3
2. P→P2O5→H3PO4→Na3PO4→Ca3(PO4)2
3. Zn→ZnCl2→Zn(OH)2→ZnO→Zn(NO3)2
4.Cu →CuO→CuCl2→Cu(OH)2→CuO→Cu
5.N2O5→HNO3→Fe(NO3)2→Fe(OH)2→FeS→FeSO4
V. Тренажёры
Тренажёр №1. «Классы неорганических соединений»
Тренажёр №2. «Генетическая связь между классами неорганических веществ»
Задание:
Прочитайте отрывок из романа Л. Буссенара «Похитители бриллиантов» и выполните задания:
«Пожар пылал несколько часов подряд. Пещера превратилась в настоящую печь по обжигу извести. Неслыханной силы пламя обожгло весь известковый пласт, который представляет собой углекислую соль кальция. Под действием огня известняк разложился, угольная кислота выделилась, и получилось именно, то, что называется негашеной известью. Оставалось только, чтобы на нее попало известное количество воды.
Так и случилось. Ливень, который последовал за грозой, залил всю эту огромную массу негашеной извести, она разбухла, стала с непреодолимой силой распирать сжимавший её уголь и выталкивать его по направлению к пропасти… Скалы, деревья, клад, мумии – все исчезло в мгновение ока вместе с презренными негодяями».
Задания:
- Составить и осуществить цепочку превращений.
- Решить задачу.
- Определить массу негашеной извести, образующейся при разложении известняка массой 300г., в котором массовая доля некарбонатной примеси составляет 20%.
Лабиринт
Пять человек отправляются в путешествие в царство Солей. Если формула вещества соответствует приведенному под ней названию, то вы переходите к следующему пункту по стрелке «да», если не соответствует – по стрелке «нет». Можно войти в любой «вход». Но правильный «выход» только один – «пункт Г».
ЦОРы
Учебный видео-фильм: “Генетическая связь между отдельными классами неорганических соединений”
Из веществ одного класса можно получить вещества другого класса. Такую связь, отражающую происхождение веществ, называют генетической (от греч. «генезис» — происхождение). Рассмотрим сущность генетических связей между классами неорганических веществ.
В ходе химических реакций химический элемент не исчезает, атомы переходят из одного вещества в другое. Атомы химического элемента как бы передаются от простого вещества к более сложному, и наоборот. Таким образом, возникают так называемые генетические ряды, начинающиеся простым веществом – металлом или неметаллом – и заканчивающиеся солью.
Напомню вам, что в состав солей входят металлы и кислотные остатки. Итак, генетический ряд металла может выглядеть таким образом:
Из металла в результате реакции соединения с кислородом можно получить основный оксид, основный оксид при взаимодействии с водой дает основание (только, если это основание – щелочь), из основания в результате реакции обмена с кислотой, солью или кислотным оксидом можно получить соль.
Обратите внимание, такой генетический ряд подходит только для металлов, гидроксиды которых являются щелочами.
Запишем уравнения реакций, соответствующих превращениям лития в его генетическом ряду:
Li → Li2O → LiOH→ Li2SO4
Как вы знаете, металлы при взаимодействии с кислородом, как правило, образуют оксиды. При окислении кислородом воздуха литий образует оксид лития:
4Li + O2 = 2Li2O
Оксид лития, взаимодействуя с водой, образует гидроксид лития – растворимое в воде основание (щелочь):
Li2O + H2O = 2LiOH
Сульфат лития можно получить из лития несколькими способами, например, в результате реакции нейтрализации с серной кислотой:
2LiOH + H2SO4 = Li2SO4 + 2H2O
2. Генетический ряд неметалла
Составим теперь генетический ряд неметалла:
Неметалл образует кислотный оксид. Из кислотного оксида при реакции с водой образуется кислота. Из кислоты в результате взаимодействия с металлом, основанием, солью или основным оксидом можно получить соль.
В качестве примера рассмотрим последовательные превращения серы:
S → SO2 → H2SO3 → K2SO3
Для получения оксида серы(IV) нужно провести реакцию горения серы в кислороде:
S + O2 = SO2
При растворении оксида серы(IV) в воде образуется сернистая кислота:
SO2 + H2O = H2SO3
Сульфит калия из сернистой кислоты можно получить, например, в результате реакции с основным оксидом — оксидом калия:
K2O + H2SO3 = K2SO3 + H2O
Другой способ получения сульфита калия из сернистой кислоты – реакция нейтрализации с гидроксидом калия:
2KOH + H2SO3 = K2SO3 + 2H2O
3. Реакции между представителями двух генетических рядов
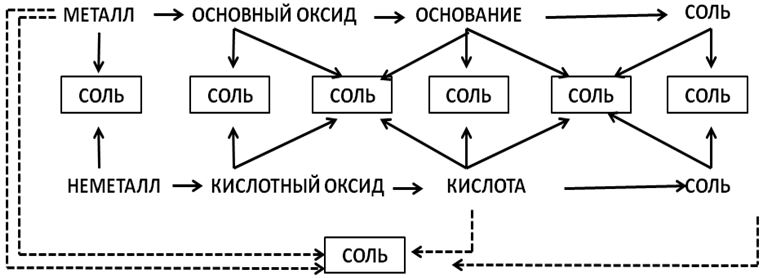
Генетическая связь между классами неорганических веществ приведена на Рис. 1.
Рис. 1. Генетическая связь между классами неорганических веществ
В приведенной схеме пары стрелок, направленных навстречу друг другу, показывают, какие реагенты нужно взять, чтобы получить соль.
Например, соль образуется при взаимодействии металла и неметалла, основного оксида и кислоты, металла и кислоты и т.д.
Запомним, что характерными являются реакции между представителями разных генетических рядов. Вещества из одного генетического ряда, как правило, не вступают во взаимодействия.